Le cochon, une source intarissable pour le don d’organes ?
La pénurie d’organes est un frein considérable aux greffes entre humains. Pour y palier, les chercheurs se tournent vers d’autres espèces, comme… le cochon. Une équipe internationale vient de publier dans Science ses résultats sur l’inactivation d’un virus porcin transmissible du greffon au receveur. Leur succès constitue une avancée considérable pour la xénotransplantation.
La xénogreffe : enjeux et écueils
Le don d’organes ou de tissus humains constitue l’un des besoins médicaux les moins satisfaits tant la demande dépasse de loin l’offre. En effet, comme l’indique le Dr David Klassen, médecin en chef de l’organisme américain United Network for Organ Sharing, la majorité des prélèvements d’organes sont réalisés sur des personnes en état de « mort cérébrale ». Il ajoute que cette année aux Etats-Unis, près de 17157 organes ont été greffés bien loin des 116800 patients inscrits sur liste d’attente. Les scientifiques voient donc en la xénogreffe, la greffe entre espèces différentes, une potentielle ouverture médicale afin de pallier au faible nombre de donneurs humains.
A noter ! Les données 2016 pour la France selon le communiqué de presse du 20 mars 2017 de l’agence de la biomédecine : 5891 organes ont été greffés et 22617 patients sont toujours sur liste d’attente.
Ce type de greffe, plus encore que celle issue de donneurs humains, se heurte à la barrière immunitaire du receveur qui peut attaquer le greffon et entraîner son rejet par l’organisme. A cela s’ajoute la possibilité de la transmission de virus potentiellement mortels entre le greffon et le receveur.
Entre le porc et l’homme, il n’y a qu’un gène… ou presque
Plus le patrimoine génétique du donneur est proche de celui du receveur et plus le risque de rejet est moindre. Aussi, les premières xénogreffes envisagées ont impliqué des organes issus de primates, mais leur faible nombre et la classification de certains comme espèces protégées, comme les chimpanzés, ont imposé la recherche d’une autre source.
Le Sus scrofa domesticus, ou cochon domestique, élevé à grande échelle, semble une alternative toute trouvée. Jusque dans les années 80, il était le premier fournisseur d’insuline injectée aux patients, et actuellement des recherches sont menées pour implanter des cellules pancréatiques de porc pour des patients atteints de diabète de type I. Il possède également des organes anatomiquement proches de celui de l’Homme, notamment le cœur, dont actuellement on prélève les valves pour les implanter dans des cœurs humains.
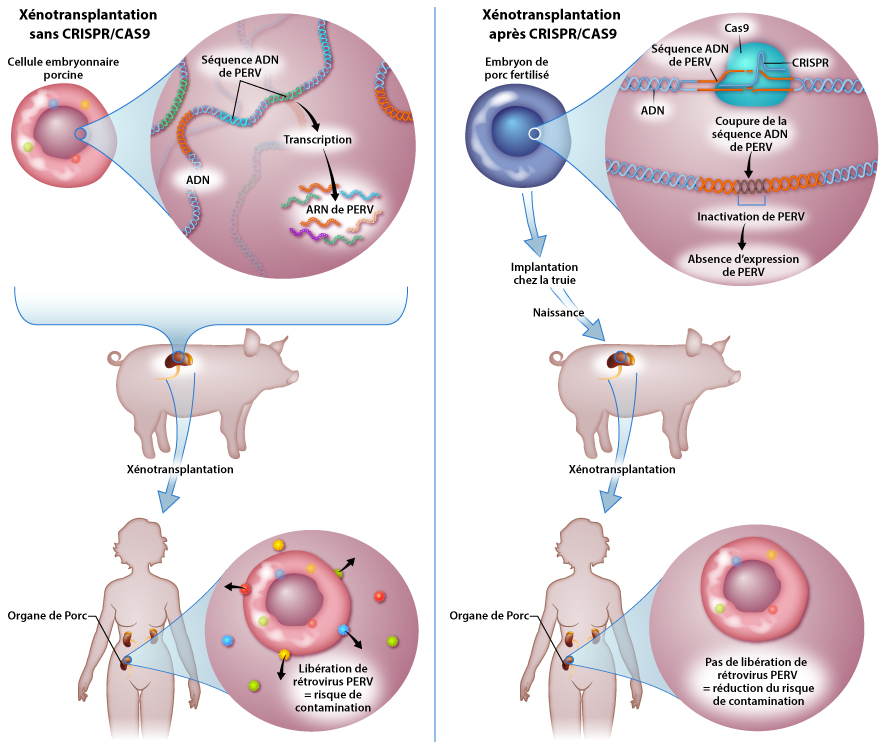
Cette solution de xénogreffe est jusqu’à maintenant expérimentale, principalement à cause d’un risque important de rejet systémique du greffon par le receveur. Le second frein concerne également le risque de transmission de rétrovirus, les PERV (Porcine Endogenous Retrovirus), des séquences présentes dans l’ADN du porc et qui peuvent s’intégrer à l’ADN du receveur humain. La crainte est que ces rétrovirus, dont les généticiens ont clairement identifié les gènes intégrés à l’ADN de porc, possèdent des séquences similaires à celles de rétrovirus provoquant des leucémies chez le Singe et qu’ils puissent être potentiellement dangereux pour l’homme après transplantation.
Lire aussi – Bientôt des cochons porteurs d’organes humains
La technique CRISPR-CAS9 au secours de la xénogreffe
La très médiatisée technique CRISPR-CAS9, ou « édition génomique », doit sa renommée aux possibilités de modification génétique qu’elle offre.
A savoir ! La technologie CRISPR CAS9 permet, grâce à un complexe protéique et une séquence d’ARN dite « guide », de cibler une séquence d’ADN spécifique et de la découper. Il est alors possible d’inactiver un gène ou d’introduire un nouveau gène.
Grâce à cette technique, les chercheurs ont réussi à retirer de l’ADN des embryons de porc, les gènes codant pour des rétrovirus porcins. Ils ont ensuite inséminé plusieurs truies qui ont donné naissance à 37 porcelets n’exprimant pas de PERV dans leur organisme. Une fois matures, leurs organes seront potentiellement compatibles pour une xénotransplantation.
Parmi les chercheurs, on peut citer les Dr George M. Church et Luhan Yang, co-fondateurs de la société eGenesis dont l’objectif est la commercialisation d’organes génétiquement modifiés de porc. Ils dirigent également leur recherche vers la diminution des marqueurs cellulaires reconnus par le système immunitaire du receveur et entraînant les rejets du greffon.
Maintenant, les patients sont-ils prêts à accepter la transplantation d’un organe issu d’un animal, d’autant plus du porc ? Pour information : un rapport français de Michel Fellous pour l’établissement français des greffes, paru en 2003, précise que moins de la moitié des patients interrogés seraient prêt à recevoir une xénogreffe, choix à pondéré avec l’urgence vitale de leur situation.
Romain R., Docteur en Biologie Moléculaire et Cellulaire
Cet article vous a-t-il été utile ?