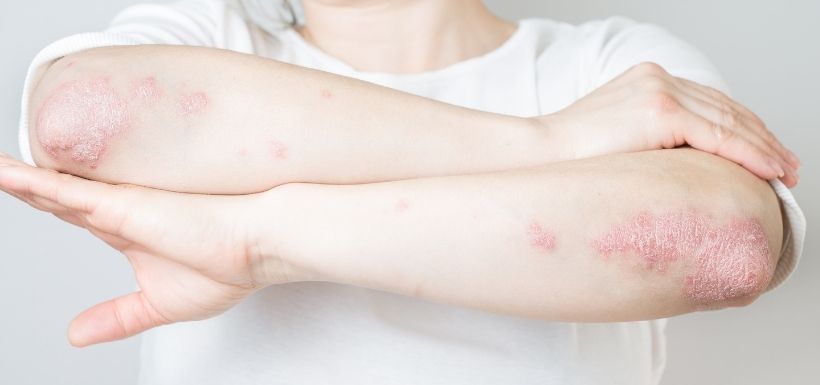
Psoriasis : Vers une nouvelle stratégie thérapeutique ?
Touchant 2 à 3% des français, le psoriasis désigne une maladie inflammatoire chronique de la peau liée à la sécrétion de substances impliquées dans l’inflammation. Et s’il était possible d’en réduire les manifestations grâce à une nouvelle stratégie thérapeutique ? C’est ce que suggèrent les travaux d’une équipe de chercheurs de l’Inserm.
Psoriasis : de la nécessité de nouveaux traitements
Des plaques rouges recouvertes de squames constituent un symptôme caractéristique d’une maladie inflammatoire chronique de la peau appelée psoriasis. Ces lésions se situent généralement au niveau des mains, des coudes, des genoux, du bas du dos, ou encore sur le visage et le cuir chevelu. Elles ne provoquent que peu ou pas de démangeaisons.
À savoir ! Le psoriasis est généralement une maladie bénigne. Il existe cependant des formes sévères (dans 20 % des cas) associées à une atteinte généralisée et/ou à des douleurs articulaires.Ces lésions inflammatoires sont liées à un dérèglement immunitaire qui entraîne l’infiltration de cellules immunitaires dans les couches moyennes et superficielles de la peau (le derme et l’épiderme). Parmi ces cellules immunitaires appartenant à la famille des lymphocytes T, on peut citer les lymphocytes Th17 dont le rôle consiste à produire des substances impliquées dans l’inflammation appelées cytokines (comme l’IL-17, IL-22, IFNg, TNFα…). Cette inflammation chronique et exagérée de la peau cause alors une hyperprolifération pathologique des cellules de l’épiderme, ce qui augmente l’épaisseur de la couche cornée de la peau.
A l’heure actuelle, il n’est pas possible de guérir cette maladie. Les principaux traitements permettent seulement d’en réduire les symptômes et d’améliorer la qualité de vie des patients (pommades anti-inflammatoires, traitements par voie orale…). En cas de psoriasis résistant, c’est alors la biothérapie qui est envisagée. Les traitements consistent à cibler le processus inflammatoire grâce à des anticorps monoclonaux thérapeutiques dirigés contre les cytokines pro-inflammatoires (IL-17, l’IL-22 ou le TNFα). C’est sans compter les inconvénients de taille de ces traitements : prix excessivement élevé, administration par voie sous-cutanée nécessitant l’intervention d’un spécialiste et risque d’effets indésirables.
C’est dire combien trouver des alternatives thérapeutiques s’avère être un enjeu crucial pour le monde scientifique. Dans ce contexte, les travaux d’une équipe de chercheurs toulousains de l’Inserm suggèrent une nouvelle piste de traitement.
Le rôle clé du canal calcique dans le processus inflammatoire
De précédents travaux avaient démontré que les lymphocytes Th17 présents dans la circulation sanguine exprimaient à leur surface un canal calcique particulier appelé Cav1.4. Ce canal calcique joue un rôle essentiel en ce sens qu’il permet la production des cytokines, les fameuses substances pro-inflammatoires. Or, il s’avère que ce canal calcique est spécifique des lymphocytes Th17. Ce qui signifie qu’on ne le retrouve pas sur d’autres types de lymphocytes.
A l’occasion de cette nouvelle étude, la chercheuse Magali Savignac et ses collègues ont souhaité vérifier la présence de ces canaux calciques Cav1.4 à la surface des lymphocytes Th17 qui infiltrent la peau des patients atteints de psoriasis.
Pour mener à bien leurs recherches, les scientifiques ont eu recours à des biomarqueurs spécifiques pour repérer les cellules Th17 et visualiser le canal Cav1.4 à leur surface. L’objectif de l’étude consistait à bloquer ce canal pour observer les conséquences sur la production de cytokines dans différents modèles d’étude du psoriasis. Les scientifiques ont donc utilisé une molécule déjà connue pour ses propriétés d’inhibition des canaux Cav1 des vaisseaux sanguins : la nicardipine.
À savoir ! La nicardipine est un produit déjà commercialisé dans le traitement de l’hypertension.En travaillant sur des lymphocytes Th17 issus d’échantillons sanguins de patients atteints de psoriasis ou de sujets sains, puis de biopsies cutanées de patients, les chercheurs ont pu observer les résultats suivants :
- Chute de la production de cytokines (IL-17, IL-22, IFNg et TNFα) par les lymphocytes Th17 en présence de nicardipine.
- Même conclusion avec un modèle de souris atteintes d’un psoriasis induit.
Vers une nouvelle stratégie thérapeutique ?
Les chercheurs sont ensuite allés plus loin en reconstituant un modèle de peau humaine, en culture en 3D à partir de cellules saines. Après y avoir inséré des lymphocytes Th17, ils ont pu observer qu’ils infiltraient la peau en culture provoquant l’apparition de signes de psoriasis en quelques jours. En revanche, les signes de psoriasis n’apparaissaient pas si les lymphocytes Th17 avaient été préalablement exposés à la nicardipine !
Pour l’équipe de chercheurs, ces résultats prouvent que les lymphocytes Th17 qui infiltrent la peau dans le psoriasis expriment bien le canal calcique Cav1.4 et que le blocage de ce canal réduit la production locale de cytokines inflammatoires. Selon eux, bloquer ce canal pourrait donc permettre de lutter contre l’inflammation et réduire les manifestations du psoriasis. Cette découverte ouvre des perspectives prometteuses quant au développement de nouvelles stratégies thérapeutiques aptes à réduire les symptômes du psoriasis.
Déborah L., Docteur en Pharmacie
Cet article vous a-t-il été utile ?